Du brassard au cloud : l’impact concret de l’évaluation artérielle connectée
L’artériopathie oblitérante des membres inférieurs (AOMI) reste sous-diagnostiquée. Ici, nous explorons comment des solutions connectées comme le MESI mTABLET ABI et TBI simplifient le dépistage de l’AOMI des cabinets de soins primaires aux programmes nationaux de dépistage.
Une maladie en expansion mais négligée
La prévalence mondiale de l’artériopathie oblitérante des membres inférieurs augmente à un rythme alarmant. En 2019, on estimait à 113 millions le nombre de cas d’AOMI, soit une augmentation de 72,5 % par rapport à 1990 où seulement 65 millions de personnes étaient touchées par cette maladie souvent silencieuse [1]. Certaines études épidémiologiques suggèrent des chiffres encore plus élevés (236,62 millions de cas signalés en 2015 [2]). En outre, les projections indiquent qu’en 2050, le nombre de personnes atteintes d’AOMI pourrait atteindre au moins 360 millions, accompagné d’un doublement de la mortalité standardisée selon l’âge et d’une augmentation spectaculaire des années de vie ajustées sur l’incapacité ou DALY (de 19,7 à 33,1 pour 100 000, par rapport aux données de 2021) [3].
Cette tendance inquiétante est principalement due à la prévalence croissante des maladies métaboliques, en particulier le diabète [3]. Les personnes diabétiques ont 2 à 3 fois plus de risques de développer une AOMI que les non-diabétiques, et près de 50 % des patients atteints d’ulcères du pied diabétique souffrent également d’AOMI [4], [5], [6]. Cette comorbidité augmente considérablement la morbidité et la mortalité prématurée et est associée à un risque accru d’ischémie critique des membres (ICM), la forme la plus grave de l’AOMI, avec des taux de prévalence (chez les patients diabétiques) atteignant jusqu’à 76 % [7]. Les diabétiques atteints d’ICM présentent également de moins bons résultats (taux plus élevés d’amputations des membres inférieurs et de mortalité) que ceux atteints d’une seule de ces pathologies. Ils ont un risque d’amputation majeure 5 à 15 fois plus élevé que ceux atteints d’AOMI seule – l’ICM elle-même est associée à des taux d’amputation de 10 à 40 % dans les six mois suivant le diagnostic et à des taux de mortalité de 20 % sur la même période, atteignant 50 % dans les cinq ans [8], [9], [10], [11], [12].
En général, l’ICM se développe progressivement et est souvent précédée de claudication intermittente, un symptôme de l’AOMI à un stade précoce. Cependant, seulement 10 % des patients atteints d’AOMI présentent ce symptôme, tandis que 40 % restent asymptomatiques et 50 % présentent des symptômes atypiques pouvant être attribués à d’autres affections [13], [14]. Bien que les diabétiques présentent un risque plus élevé de claudication intermittente (les hommes ayant un risque 3,5 fois plus élevé, et les femmes un risque 8,6 fois plus élevé que les non-diabétiques), cela a une utilité diagnostique limitée en ce qui concerne l’AOMI, car les patients diabétiques font déjà l’objet d’un suivi médical plus étroit et sont plus susceptibles de recevoir un diagnostic d’AOMI en temps opportun [15].
Un autre problème de la claudication intermittente est sa tendance à être confondue avec des affections courantes liées à l’âge telles que l’arthrite. L’arthrite et l’AOMI partagent plusieurs facteurs de risque, comme l’âge avancé et l’obésité, ce qui peut retarder le diagnostic et le traitement précis [16], [17], [18]. En plus de l’arthrite, la claudication intermittente peut également être confondue avec d’autres affections telles que la sciatique, la maladie athéroembolique, l’insuffisance veineuse et la vascularite [19]. Enfin, malgré les efforts croissants pour sensibiliser à l’AOMI et à ses symptômes, la compréhension du public reste limitée [20], [21], [22], [23]. De nombreuses personnes ne sont diagnostiquées qu’une fois la maladie à un stade avancé, ce qui souligne la nécessité d’une reconnaissance et d’une intervention plus précoces.
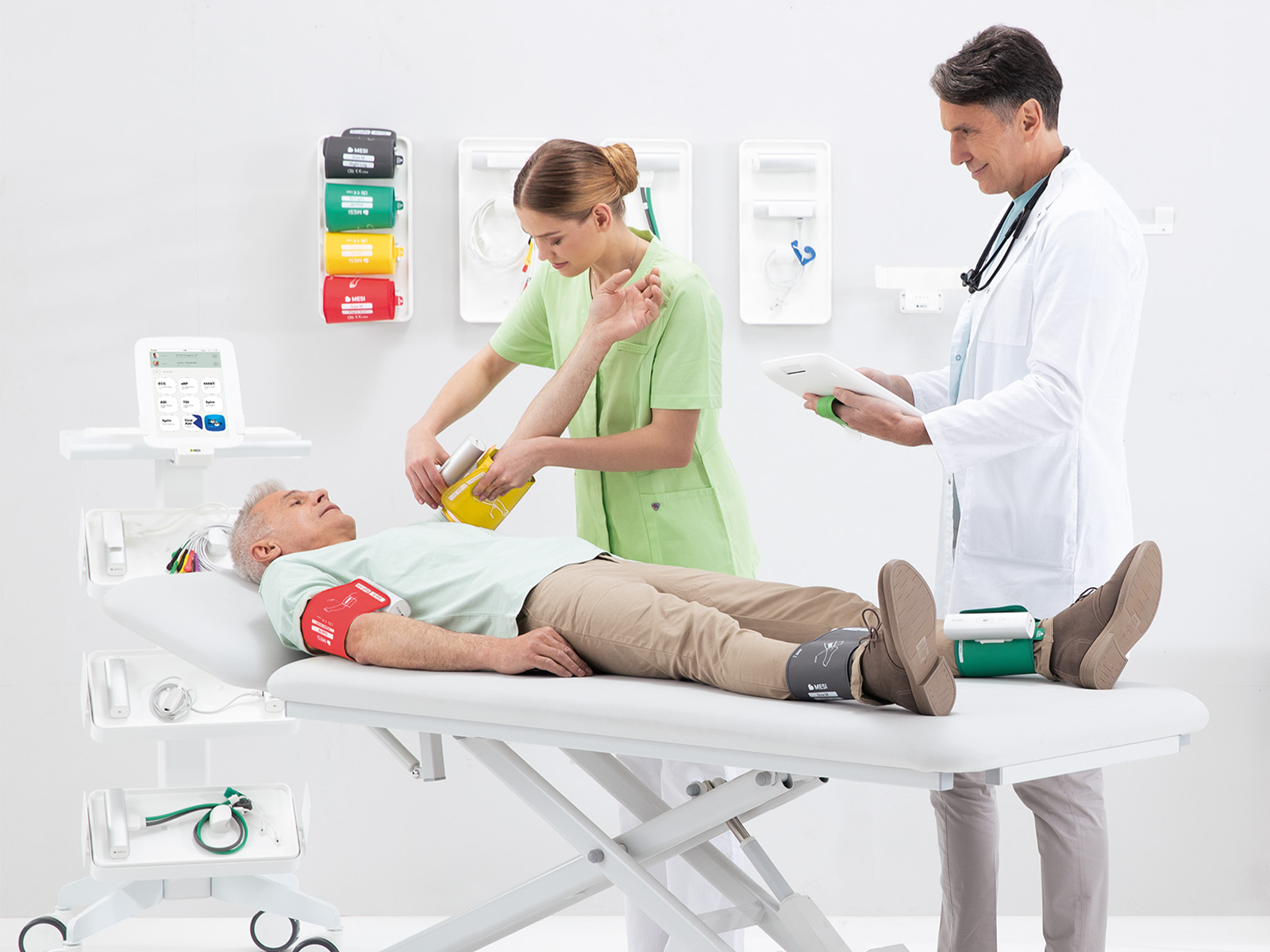
IPS et IPSO : des outils simples aux informations puissantes
D’un point de vue diagnostique, l’indice de pression systolique (IPS) est l’alternative de choix. Par rapport aux divers questionnaires patients peu fiables ou à des techniques d’imagerie plus fiables et précises mais complexes comme l’angiographie par tomodensitométrie (CTA), l’angiographie par résonance magnétique (MRA) ou l’échographie, l’IPS est non invasif, rapide, économique et adapté aux structures ambulatoires [24], [25], [26], [27], [28], [29]. De plus, au-delà du diagnostic de l’AOMI et de l’évaluation de sa gravité, l’IPS a également une valeur diagnostique supplémentaire.
Les recherches ont montré qu’un IPS faible ou autrement anormal est un indicateur fort d’athérosclérose systémique, non seulement aux membres inférieurs mais aussi au niveau des lits artériels coronaires et non coronaires (c’est-à-dire autres que ceux des membres inférieurs) [30]. Un IPS réduit est également associé à un risque accru d’accident vasculaire cérébral ischémique, et le score d’IPS en général est un indicateur important de la santé cardiovasculaire globale, pouvant améliorer la précision de la prédiction du risque cardiovasculaire au-delà du FRS (score de risque de Framingham). [31], [32]. L’IPS est également déterminant pour le diagnostic et l’orientation du traitement des ulcères d’insuffisance veineuse et artérielle – les deux types d’ulcères des membres inférieurs les plus fréquents [33]. Ils peuvent (visuellement) se ressembler, mais leurs mécanismes physiopathologiques diffèrent et exigent des approches thérapeutiques distinctes, parfois mutuellement exclusives. Heureusement, on peut les différencier grâce à l’IPS. Un IPS entre 0,8 et 1,2 évoque une insuffisance veineuse, un IPS plus bas entre 0,51 et 0,79 suggère des ulcères mixtes veineux/artériels, tandis qu’une valeur de 0,5 ou moins est compatible avec une AOMI [34].
L’IPS est toutefois inutilisable chez les personnes présentant des artères incompressibles, le plus souvent dues à une calcification médiale des artères (également appelée sclérose de Mönckeberg), que l’on retrouve chez les personnes atteintes de diabète, d’insuffisance rénale et de polyarthrite rhumatoïde [35], [36], [37], [38]. La mesure de l’IPS chez ces patients renverra probablement une valeur anormalement élevée (généralement ≥ 1,30), ce qui suggère une mortalité plus élevée et un risque accru d’infarctus du myocarde par rapport à ceux ayant un IPS normal, mais n’apporte aucune information utile sur la présence ou la gravité de l’AOMI [39], [40]. Heureusement, les artères des orteils sont rarement touchées par la calcification, ce qui les rend adaptées à la mesure de la pression artérielle – c’est-à-dire l’évaluation de l’indice de pression systolique de l’orteil (IPSO) – réalisée de manière similaire à l’IPS, mais avec des brassards de pression beaucoup plus petits (pour les orteils) [41]. L’IPSO est également préférable chez les personnes souffrant de douleurs excruciantes aux membres inférieurs (en raison d’ulcères ou d’autres causes) [42], [43].
Comme l’IPS, l’IPSO apporte des informations diagnostiques au-delà du dépistage de l’AOMI. Un IPSO bas est associé à un risque accru de récidive de maladie cardiovasculaire et à la progression de la néphropathie diabétique chez les patients atteints de diabète de type 2 ; c’est aussi un prédicteur informatif de la mortalité chez les patients en dialyse [44], [45], [46].
Cependant, lorsqu’on choisit entre une évaluation par IPS ou par IPSO pour un patient donné, il est important de considérer que la calcification médiale des artères peut masquer une AOMI sous-jacente en élevant artificiellement les valeurs d’IPS dans la plage normale [47]. Par conséquent, la réalisation conjointe de l’IPS et de l’IPSO est recommandée chez les personnes susceptibles de présenter une calcification artérielle d’après leurs antécédents médicaux. Cette approche nécessite l’accès à deux dispositifs diagnostiques distincts – ou, idéalement, à un appareil polyvalent unique offrant des fonctionnalités étendues qui intègre la mesure de l’IPS et de l’IPSO avec un système de dossier de santé électronique (EHR), faisant entrer l’évaluation complète de l’AOMI dans l’ère numérique.
Comment le MESI mTABLET réunit l’ensemble
Comme le montre un nombre croissant d’études, une évaluation complète de l’AOMI n’est plus une procédure optionnelle mais une nécessité clinique [48]. Heureusement, avec des outils avancés comme le MESI mTABLET, ce processus devient nettement plus fluide qu’avec les méthodes traditionnelles utilisant une sonde Doppler et un sphygmomanomètre. Bien que l’évaluation Doppler reste précise et fiable entre des mains expertes, elle est également chronophage puisqu’elle prend généralement jusqu’à 30 minutes par patient [49].
À l’inverse, la méthode oscillométrique-pléthysmographique, telle qu’utilisée par le MESI mTABLET ABI & MESI mTABLET TBI, fournit des résultats en à peine une minute, ce qui change la donne pour le dépistage de l’AOMI [50].

Qu’il soit déployé dans un cabinet de soins primaires local ou dans le cadre d’une initiative nationale visant à améliorer le dépistage précoce de l’AOMI et les résultats pour les patients, le MESI mTABLET offre une facilité d’utilisation et une efficacité incomparables. Mesurer l’IPS ou l’IPSO ne requiert aucune formation spécialisée au-delà de la connaissance de l’emplacement des brassards – ce que la tablette elle-même facilite via un guide intuitif à l’écran. De plus, l’IPS et l’IPSO sont réalisés avec le même appareil.
Surtout, tous les résultats obtenus via l’IPS, l’IPSO ou d’autres modules diagnostiques, ou saisis manuellement dans la tablette, sont automatiquement stockés dans le dossier de santé électronique (EHR) du patient via le système cloud MESI mRECORDS. Cela garantit des données sauvegardées en toute sécurité, facilement accessibles et partageables entre professionnels de santé depuis tout appareil connecté au web. Le système offre également de nombreux autres avantages liés aux EHR, comme l’amélioration de la précision et de la fiabilité des données grâce à l’élimination des erreurs d’écriture manuscrite, ce qui réduit le risque d’erreurs médicales [51], [52]. Cependant, l’accessibilité accrue aux informations du patient reste l’avantage principal et s’avère déterminante dans le contexte de l’AOMI, où une prise en charge efficace nécessite souvent une collaboration pluridisciplinaire.
Les patients atteints d’AOMI présentent fréquemment des comorbidités telles que le diabète, la maladie rénale chronique et des plaies chroniques qui interagissent de manière complexe et s’auto-entretiennent [53], [54], [55]. De ce fait, des soins optimaux peuvent impliquer un chirurgien vasculaire, un diabétologue, un néphrologue et un spécialiste des plaies – échangeant les données médicales du patient via mRECORDS pour formuler un plan thérapeutique personnalisé visant à améliorer les résultats et à réduire les coûts, souvent substantiels, de la prise en charge des cas d’AOMI (avancés) [56], [57], [58], [59].
La réduction du fardeau de l’AOMI repose donc sur deux piliers clés : un diagnostic en temps opportun et un traitement coordonné et multidisciplinaire. Le MESI mTABLET, avec sa rapidité, sa facilité d’utilisation et son intégration intelligente, est idéalement positionné pour soutenir les deux.